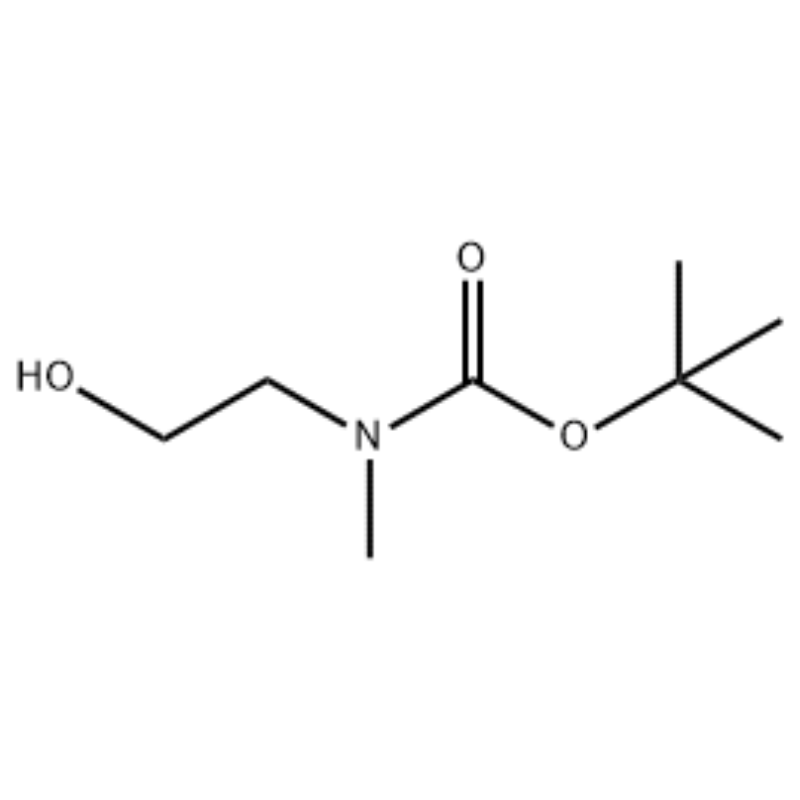
Do roztworu 2-(metyloamino)etanolu (500 mg, 0,53 ml, 6,66 mmol) w CH2Cl2 (20 ml) dodano Boc2O (1,48 g, 6,79 mmol), a następnie mieszano w temperaturze pokojowej przez 1 godzinę.Roztwór reakcyjny ekstrahowano solanką i CH2Cl2.Otrzymaną w ten sposób warstwę organiczną wysuszono nad MgSO4 i przesączono.Następnie przesącz zatężono pod próżnią i otrzymano żądany związek (bezbarwny olej, ilościowo);1H NMR (200 MHz, CDCl3) delta 3,74 (q, J= 10,5, 5,2 Hz, 2H) 3,25 (t, J= 5,2 Hz, 2H) 2,91 (s, 3H) 1,45 (s, 9H);widmo masowe m/e (natężenie względne) 144 (20) 102 (24) 57 (70) 44 (100).
Przykład 38;N1-(3-Fluoro-4-(2-(1-(2-(metyloamino)etylo)-1H-imidazol-4-ilo)tieno[3,2-b]pirydyn-7-yloksy)fenylo)-N3 -(2-metoksyfenylo)malonamid (96);Etap 1: 2-hydroksyetylo(metylo)karbaminian tert-butylu (97) (J. Med. Chem., 1999, 42, 11, 2008) Do roztworu 2-(metyloamino)etanolu (5,0 g, 67 mmol) w Dodano THF (50 ml) w temperaturze pokojowej Boc2O (15,7 g, 72 mmol) i mieszaninę reakcyjną mieszano w temperaturze pokojowej przez 4 godziny.Mieszaninę reakcyjną zatężono do sucha i tytułowy związek 97 użyto bezpośrednio w następnym etapie bez dodatkowego oczyszczania (11,74 g, wydajność 100%).MS (m/z): 176,2 (M+H).
Wytwarzanie l-2-[4-Bromo-2-(4-okso-2-ftiotaioxo1hiazolidyn-5-ylidenemefliylo)fenoksy]efliylo-3-efliylo-1-metylomocznika (Compoiotamd 161) Etap 1: Synteza t-butylu2- hydroksyetylometylokarbaminian;Do roztworu 2-(metyloamino)etanolu (500 mg, 0,53 ml, 6,66 mmol) w CH2Cl2 (20 ml) dodano BoC2O (1,48 g, 6,79 mmol), a następnie mieszano w temperaturze pokojowej przez 1 godzinę.Roztwór reakcyjny ekstrahowano solanką i CH2Cl2.Otrzymaną w ten sposób warstwę organiczną wysuszono nad MgSO4 i przesączono.Następnie przesącz zatężono pod próżnią, w wyniku czego otrzymano żądany związek (bezbarwny olej, ilościowo); 1HNMR (200 MHz, CDCl3) delta 3,74 (q, J= 10,5, 5,2 Hz, 2H) 3,25 (t, J= 5,2 Hz, 2H) 2,91 (s, 3H) 1,45 (s, 9H);widmo masowe m/e (natężenie względne) 144 (20) 102 (24) 57 (70) 44 (100).
2-(metyloamino)etanol (90,1 g, 1,2 mol) rozpuszczono w 1,2 l chlorku metylenu i powoli dodano BoC2O (218 g, 1 mol), mieszając w temperaturze 0°C, a następnie w temperaturze pokojowej przez 3 godziny.Mieszaninę reakcyjną przemyto kolejno 700 ml wodnego nasyconego roztworu chlorku amonu i 300 ml wody.Przemytą mieszaninę odwodniono za pomocą bezwodnego siarczanu sodu i zatężono pod zmniejszonym ciśnieniem, aby otrzymać związek (a) (175 g, 1 mol, 100%) w postaci bezbarwnego oleju. TLC: Rf = 0,5 (50% EtOAc w Hex) wizualizowano za pomocą barwienia Ce-Mo. 1H NMR (600 MHz, CDCl3) delta 1,47 (s, 9H), 2,88 (brs, IH), 3,41 (brs, 2H), 3,76 (brs, 2H).
90,1 g (1,2 mol) 2-(metyloamino)etanolu rozpuszczono w 1,2 l chlorku metylenu, do tego powoli dodano 218 g (1 mol) Boc2O, mieszając uzyskany roztwór w temperaturze 0°C i uzyskany roztwór mieszano w temperaturze temperaturze pokojowej przez 3 godziny.Mieszaninę reakcyjną przemyto kolejno 700 ml wodnego nasyconego roztworu chlorku amonu i 300 ml wody, odwodniono bezwodnym siarczanem sodu, a następnie zatężono pod zmniejszonym ciśnieniem, otrzymując 175 g (1 mol) związku w postaci oleju achromowego zabezpieczonego Grupa Boc (wydajność: 100%).[0140] 1H NMR (600 MHz, CDCl3) delta 7,84 (br s, 2H), 7,76 (br s, 2H), 4,34 (d, J = 15,0 Hz, 2H), 3,63 (br s, 2H), 3,04 (d , J = 15,0 Hz, 3H), 1,46 (d, J = 16,2 Hz, 9H) [0141] 90 g (0,514 mol) otrzymanego związku rozpuszczono w 1,5 l tetrahydrofuranu, 88,0 g (539 mol) N- Do tego dodano hydroksyftalimid i 141 g (0,539 mol) trifenylofosfiny, powoli dodano 106 ml (0,539 mol) azodikarboksylanu diizopropylu, mieszając uzyskany roztwór w temperaturze 0°C, i powstały roztwór mieszano przez 3 godziny, podczas gdy jego temperatura była podwyższona do temperatury pokojowej.Po zatężeniu mieszaniny reakcyjnej pod zmniejszonym ciśnieniem dodano do niej 600 ml eteru izopropylowego, powstały roztwór mieszano w temperaturze 0°C przez 1 godzinę i przesączono biały stały tlenek trifenylofosfiny.Substancję stałą przemyto 200 ml eteru izopropylowego ochłodzonego do 0°C i zebrano z pierwszym przesączem, a uzyskany przesącz zatężono pod zmniejszonym ciśnieniem, otrzymując 198 g mieszaniny Związku XX i hydrazodikarboksylanu diizopropylu w stosunku mieszania 10 do 15%. (wydajność: 120%).[0142] 1H NMR (600 MHz, CDCl3) delta 7,84 (br s, 2H), 7,76 (br s, 2H), 4,34 (d, J = 15,0 Hz, 2H), 3,63 (br s, 2H), 3,04 (d , J = 15,0 Hz, 3H), 1,46 (d, J= 16,2 Hz, 9H)
 Budynek 12, nr 309, South 2nd Road, Strefa Rozwoju Gospodarczego, dystrykt Longquanyi, Chengdu, Syczuan, Chiny.
Budynek 12, nr 309, South 2nd Road, Strefa Rozwoju Gospodarczego, dystrykt Longquanyi, Chengdu, Syczuan, Chiny. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404



















.png)


